发布时间 :2022-13-01
肿瘤药物和肿瘤耐药性一直存在 “矛”和“盾”的关系。2022年9月,圣裘德儿童研究医院DR. Green研究团队在国际最权威的学术期刊之一Cell上发表了《Sublethal cytochrome c release generates drug-tolerant persister cells》一文,揭示了亚致死性细胞色素c释放产生药物耐受持久性细胞的机制。药物耐受持久性细胞会在肿瘤常规治疗以及靶向治疗中逃避细胞凋亡,是有效癌症治疗的主要非遗传障碍。
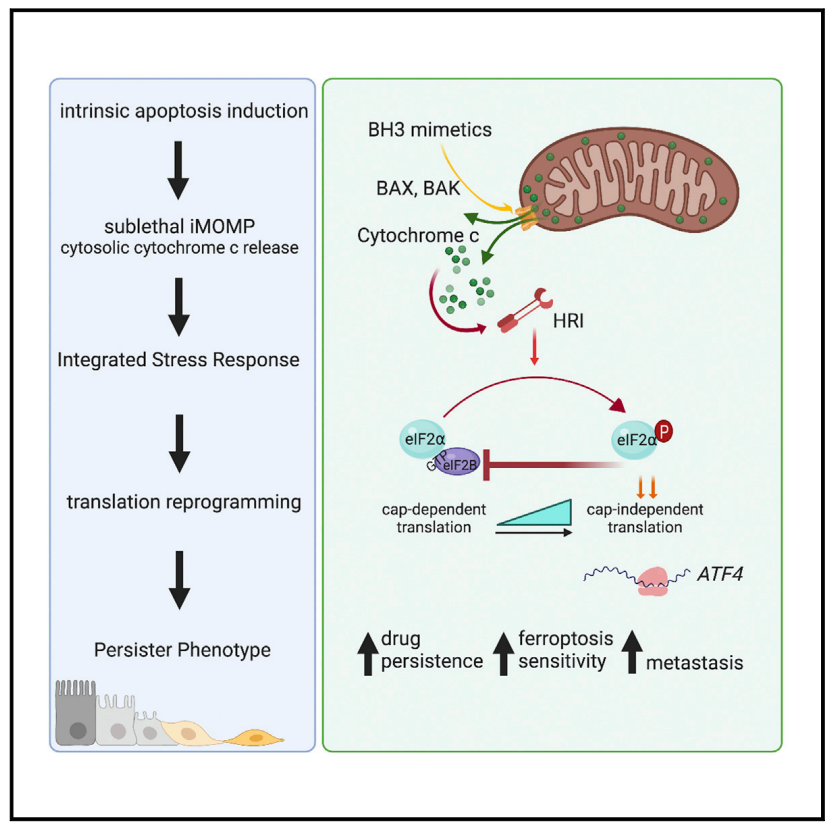
示意图:细胞色素c诱导血红素调节抑制剂(HRI)激酶的激活以及整合应激反应(ISR)的参与,促进ATF4的合成,使肿瘤细胞“逃出生天”,引发后续的不良预后。
持久性细胞系的制备
持久性细胞在功能上定义为细胞死亡诱导处理后仍然存活的细胞。研究人员发现使用针对bcl-2、bcl-xl、bcl-w的抑制剂处理后存活下来的细胞会表现出持久性表型,包括体内定植、转移以及对GPX4抑制铁死亡的敏感性增加。

首先,研究人员通过Incucyte® 实时活细胞分析系统确认了细胞给药的最大靶向剂量,然后构建了持久性细胞模型,发现持久性细胞可以使小鼠具有更高的肿瘤负荷,转移率检测发现持久性细胞具有更高的转移能力。

Incucyte® 定量分析加入1.5 mM ABT737和3 mM S63845 (S6) 抑制剂处理后,PC9 WT(野生型)细胞 、PC9 DKO (BAX和BAK双敲除)细胞、PC9 TKO(BAX、BAK和BOK三重敲除)细胞、40 mM Q-VD-OPh+ PC9 WT细胞(加入抗凋亡药物对照组)的死亡情况确认细胞给药的最大靶向剂量,400 ng/mL PI作为死细胞染料;尾静脉注射荧光素酶标记细胞的活体评估表明,注射持久性细胞的小鼠具有更高的肿瘤负荷。
接下来,研究人员发现持久性表型在很大程度上取决于Bcl-2家族效应蛋白,使用bcl-2、bcl-xl、bcl-w的抑制剂处理BAX、BAK和BOK(TKO)缺陷的PC9(PS)细胞,并将其与野生型PT细胞进行比较,TKO PS的肺定殖能力及转移潜力与PT细胞无显著性差异。
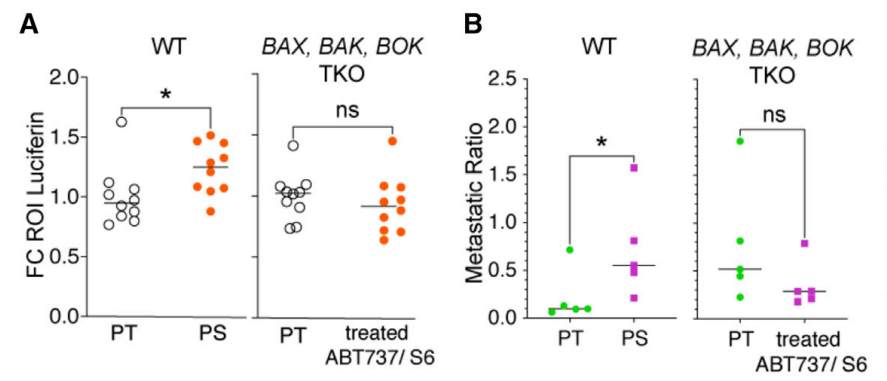
荧光素酶或CTV 、CFSE标记细胞分析表明持久性细胞表型依赖于Bcl-2。
细胞色素c-HRI-AT4通路驱动药物耐受持久性表型的产生
为了进一步了解持久性表型产生的机制,研究人员对抑制剂处理后不同时间点的PC9 PT和相应的PS进行了单细胞RNA测序。转录组学轨迹分析揭示了持久性细胞中短暂的ISR(综合应激反应)表达谱,并且确定了抑制剂诱导的ISR,依赖于Bcl-2效应蛋白,但不依赖于胱天蛋白酶激活。而且亚致死MOMP(线粒体外膜透化)的参与对ISR激活至关重要,细胞色素c激活血红素调节抑制剂 (HRI)并参与持久性表型。最终研究结果表明,细胞色素c-HRI-AT4通路驱动药物耐受持久性表型的产生。
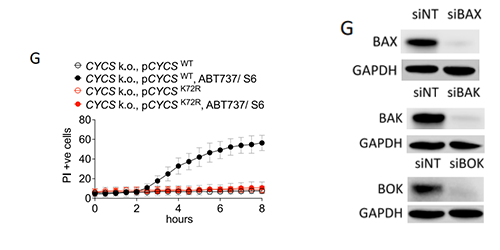
Incucyte® 分析加入1.5 mM ABT737和3 mM S6 处理细胞色素酶敲除后重新表达pCYCS WT(细胞色素酶野生型) 或者pCYCS K72R(细胞色素酶突变型)的细胞死亡情况,表明细胞色素c参与持久性表型,400 ng/mL PI作为死细胞染料。
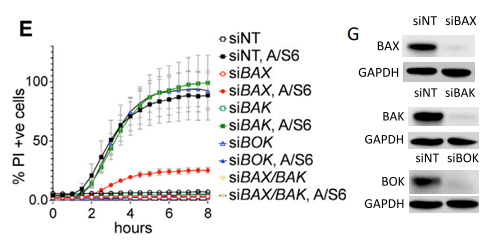
Incucyte® 定量分析1.5 mM ABT737和3 mM S6处理的单独转染或组合转染siNT、siBAX、siBAK、siBOK的 PC9细胞死亡情况,表明单独BAX的缺失几乎完全消除了对药物的敏感性,BAX为效应蛋白,400 ng/mL PI作为死细胞染料。
这一新发现解释了为什么肿瘤细胞容易对治疗药物产生耐药性,虽然不同的治疗药物作用机制可能不同,但大多数药物最终都会诱导细胞死亡,当细胞死亡被抑制,这些持久性细胞会对癌症治疗产生耐药性,本研究结果为开发通过抑制癌细胞获得持久性特征来阻止复发的药物奠定了基础。
在本研究中,研究人员多次通过Incucyte® S3实时活细胞分析系统监测与分析细胞死亡,用于确认细胞给药的最大靶向剂量、关键蛋白是否参与持久性表型等。
为什么要用Incucyte® 实时活细胞分析系统?
培养箱内可长达数周的连续观察,最短几分钟间隔拍摄,减少人力,防止过多操作对细胞的伤害;这篇文章部分实验细胞在处理8小时后就会出现明显的死亡,每30min自动对细胞进行检测,实时记录并定量分析细胞死亡情况,可以不错过实验的关键信息,并保证细胞处在稳定培养环境中;
6个板位,分别独立设置检测程序,可以兼容各种孔板和培养皿,通量高;
高效简便的模块化软件设置和数据分析,输出图片、视频、生长曲线等多指标多参数;
大于100种优化过的活细胞专用荧光试剂、耗材及详尽的Protocol。文章数大于12000篇,是长时间活细胞成像产品中最多。
电话 :

地址 :
电话 :

地址 :

地址 :